第四章 第一節(jié) 原子結(jié)構(gòu)與元素周期表——高一化學(xué)人教版(2019)必修第一冊洞悉課后習(xí)題學(xué)校:姓名:班級:考號:一、填空題1、在中:(1)和互為同位素;(2)和的質(zhì)量數(shù)相等,但不能互稱同位素;(3)和的中子數(shù)相等,但質(zhì)子數(shù)不等化學(xué)元素周期表 高清 下載,所以不是同一種元素。2、下表顯示了元素周期表中短周期的一部分,①~⑥代表6種短周期元素。① ② ③ ④ ⑤⑥已知③與氫元素能組成生活中最常見的化合物X。請?zhí)顚懴铝锌瞻住#?)與⑤同族的下一周期元素的原子結(jié)構(gòu)示意圖為。(2)④的單質(zhì)與X反應(yīng)的離子方程式為。(3)⑥的單質(zhì)與X反應(yīng)的化學(xué)方程式為。(4)①、②、③分別與氫元素組成含10個(gè)電子的分子的化學(xué)式分別為、、。3、在元素周期表中找到金、銀、銅、鐵、鋅、鈦的位置(周期和族),并指出這些元素的核電荷數(shù)。4、查閱元素周期表,從每個(gè)方格中可以得到哪些信息?以一種元素為例,將你獲得的信息用圖表示出來。
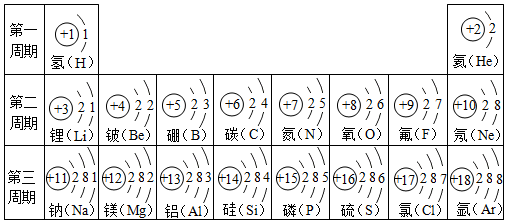
5、尋找你家中的食品、調(diào)味品、洗滌劑及清潔劑等,查找標(biāo)簽或說明書,看一看成分表中有哪些元素,找到這些元素在周期表中的位置。查閱哪些物品中含有鈉元素和鈣元素,并試著向你的家人描述它們的一些性質(zhì)或在食品中的作用。6、根據(jù)下列敘述,寫出元素名稱并畫出原子結(jié)構(gòu)示意圖。 信息 元素名稱 原子結(jié)構(gòu)示意圖 A元素原子核外M層電子數(shù)是L層電子數(shù)的一半B元素原子最外層電子數(shù)是次外層電子數(shù)的1.5倍C元素+1價(jià)離子的電子層排布與Ne相同D元素原子次外層電子數(shù)是最外層電子數(shù)的7、畫出下列元素的原子結(jié)構(gòu)示意圖:(1)某原子核內(nèi)沒有中子的元素:。(2)質(zhì)量數(shù)為23,中子數(shù)為12的原子:。(3)某元素的原子L層電子數(shù)是M層電子數(shù)的2倍:。(4)某元素原子的最外層電子數(shù)等于次外層電子數(shù)的2倍:。(5)某元素原子L層上的電子數(shù)為K層的3倍:。(6)某元素原子L層上的電子數(shù)為K層的一半:。(7)某元素原子的最外層電子數(shù)等于次外層電子數(shù):。

(8)電子總數(shù)是最外層電子數(shù)3倍的原子:。8、結(jié)合元素周期表回答下列問題:(1)表中的實(shí)線是元素周期表的部分邊界,請?jiān)趫D中用實(shí)線補(bǔ)全元素周期表的邊界。(2)表中所列元素,屬于短周期元素的有,屬于主族元素的有;g元素位于第周期族;i元素位于第周期第族。(3)元素f是第周期第族元素,請?jiān)谌缦路娇蛑邪春ぴ氐氖綐訉懗鲈撛氐脑有驍?shù)、元素符號、元素名稱、相對原子質(zhì)量。(4)元素在元素周期表中的位置與元素原子結(jié)構(gòu)的關(guān)系為。二、單選題9、考古學(xué)上常用來測定文物的年代。的原子核內(nèi)中子數(shù)是( )。A.6 B.8 C.14 D.2010、下列關(guān)于F、Cl、Br、I的比較,不正確的是( )。A.它們的原子核外電子層數(shù)隨核電荷數(shù)的增加而增多B.單質(zhì)的氧化性隨核電荷數(shù)的增加而減弱C.它們的氫化物的穩(wěn)定性隨核電荷數(shù)的增加而增強(qiáng)D.單質(zhì)的顏色隨核電荷數(shù)的增加而加深11、2016年IUPAC將第117號元素命名為Ts(中文名“”,音tion),Ts的最外層電子數(shù)是7。
下列說法中,不正確的是( )。A.Ts是第七周期第ⅦA族元素B.Ts的同位素原子具有相同的電子數(shù)C.Ts在同族元素中非金屬性最弱D.中子數(shù)為176的Ts化學(xué)元素周期表 高清 下載,其核素符號是12、“碳達(dá)峰”“碳中和”成為全國兩會的熱詞。下列有關(guān)和的說法中正確的是( )A.和的質(zhì)子數(shù)相同,互稱為同位素B.和的質(zhì)量數(shù)相同,互稱為同位素C.和的質(zhì)子數(shù)相同是同一種核素D.和的核外電子數(shù)相同,中子數(shù)不同,不能互稱為同位素13、我國“玉兔”號月球車用作為熱源材料。關(guān)于的敘述正確的是( )A.質(zhì)量數(shù)是94B.質(zhì)子數(shù)是145C.中子數(shù)為239D.核外電子數(shù)94